No estudo ATTAIN-1, o comprimido oral experimental tomado uma vez ao dia demonstrou eficácia, segurança e tolerabilidade consistentes com as terapias injetáveis de GLP-1 ao longo de 72 semanas
Orforgliprona atingiu o desfecho primário e todos os principais desfechos secundários, incluindo melhorias em fatores de risco cardiovasculares
SÃO PAULO, Agosto 7, 2025 – A Eli Lilly and Company anunciou hoje os resultados topline do estudo fase 3 ATTAIN-1 que avaliou a orforgliprona, um agonista experimental do receptor de GLP-1 (peptídeo semelhante ao glucagon 1) de administração oral em 3.127 adultos com obesidade ou sobrepeso com uma comorbidade, sem diabetes. Após 72 semanas, todas as três doses de orforgliprona atingiram o desfecho primário e todos os desfechos secundários em comparação ao placebo, proporcionando uma perda de peso clinicamente significativa como complemento a dieta saudável e atividade física. Para o desfecho primário, a orforgliprona 36 mg, administrada uma vez ao dia sem restrições quanto a alimentos ou bebidas, reduziu o peso corporal até 12,4% em comparação com 0,9% do placebo, utilizando a estimativa de eficácia1.
“A obesidade é um dos maiores desafios globais de saúde do nosso tempo, impulsionando a carga de doenças crônicas em todo o mundo e afetando mais de um bilhão de pessoas em todo o mundo. Com a orforgliprona, nós poderemos transformar o tratamento da obesidade por meio de uma terapia oral diária que poderá apoiar na intervenção precoce e tratamento a longo prazo da doença, enquanto ainda proporciona uma maior conveniência em comparação aos injetáveis. Com estes dados positivos em mãos, estamos planejando submeter a orforgliprona para avaliação regulatória até ao final do ano e preparados para um lançamento global que será capaz de atender essa demanda urgente de saúde pública.”, afirma Kenneth Custer, Ph.D. e vice-presidente executivo e presidente do negócio de Cardiometabolismo da Lilly.
No estudo ATTAIN-1, a orforgliprona atingiu o desfecho primário de redução superior do peso corporal em comparação ao placebo. Os participantes que receberam a dose mais elevada de orforgliprona perderam, em média, 12,4% do peso após 72 semanas, de acordo com a estimativa de eficácia. Em um desfecho secundário principal, 59,6% dos participantes que receberam a dose mais elevada de orforgliprona perderam pelo menos 10% do peso corporal, enquanto 39,6% perderam pelo menos 15%. Além da perda de peso significativa, a orforgliprona também foi associada à redução de conhecidos marcadores de risco cardiovacular, como colesterol não-HDL, triglicerídeos e pressão arterial sistólica nas análises agrupadas de todas as doses. Em uma análise exploratória pré-especificada, a dose mais elevada de orforgliprona reduziu os níveis de proteína C-reativa de alta sensibilidade (hsCRP) em 47,7%.
Para Luiz André Magno, Diretor Médico Sênior da Eli Lilly do Brasil, os resultados são muito animadores. “Sabemos da importância de oferecer diferentes opções terapêuticas para que médicos e pacientes possam discutir juntos pelo tratamento mais adequado para cada um, principalmente para os que não se adaptam a medicamentos injetáveis”, afirma.
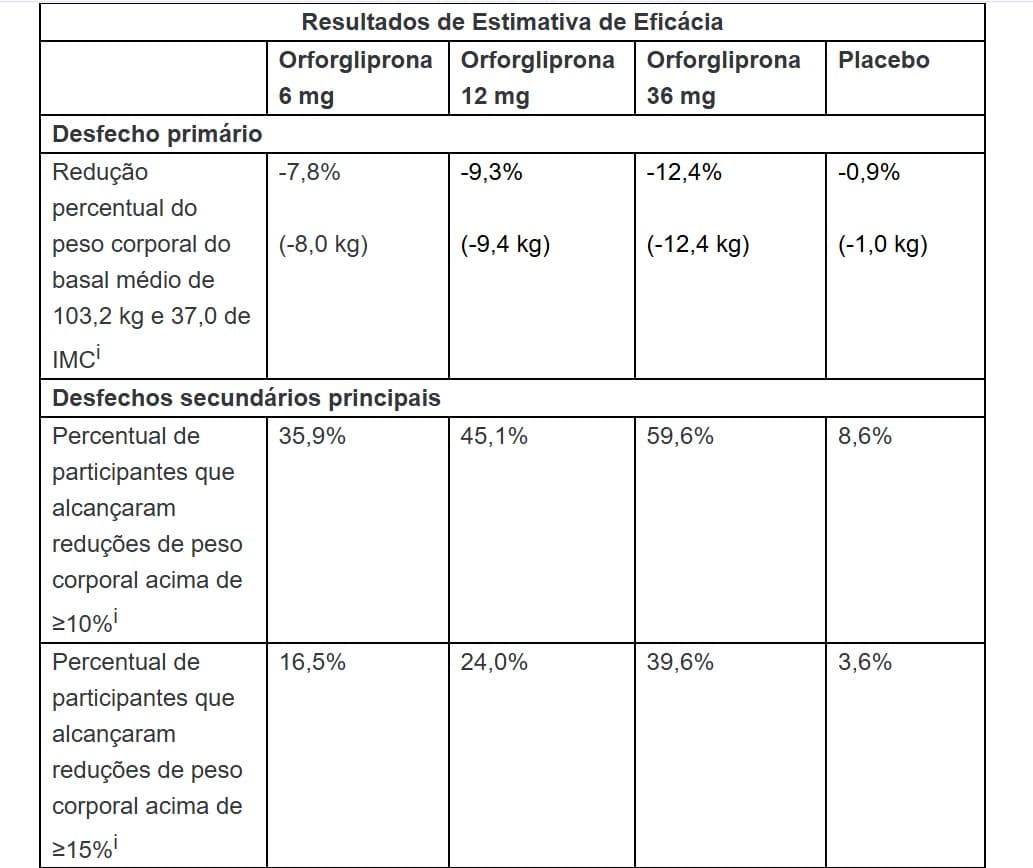
I O teste de superioridade foi ajustado para multiplicidade.
Para a estimativa de regime de tratamento2, cada dose de orforgliprona resultou em melhoras significativas nos desfechos primários e todos os principais desfechos secundários:
- Redução percentual do peso: -7,5% (-7,8 kg; 6 mg), -8,4% (-8,6 kg; 12 mg), -11,2% (-11,3 kg; 36 mg), -2,1% (-2,4 kg; placebo)
- Percentual de participantes que alcançaram reduções de peso corporal acima de ≥10%: 33,3% (6 mg), 40,0% (12 mg), 54,6% (36 mg), 12,9% (placebo)
- Percentual de participantes que alcançaram reduções de peso corporal acima de ≥15%: 15,1% (6 mg), 20,3% (12 mg), 36,0% (36 mg), 5,9% (placebo)
O perfil geral de segurança da orforgliprona no ATTAIN-1 foi consistente com o já estabelecido da classe dos agonistas do receptor GLP-1. Os eventos adversos mais frequentemente relatados foram gastrointestinais e geralmente de leve a moderada gravidade. Os eventos adversos mais comuns para participantes tratados com orforgliprona (6 mg, 12 mg e 36 mg, respectivamente) foram náusea (28,9%, 35,9% e 33,7%) vs. 10,4% com placebo, constipação (21,7%, 29,8% e 25,4%) vs. 9,3% com placebo, diarreia (21,0%, 22,8% e 23,1%) vs. 9,6% com placebo, vômitos (13,0%, 21,4% e 24,0%) vs. 3,5% com placebo, e dispepsia (13,0%, 16,2% e 14,1%) vs. 5,0% com placebo. As taxas de descontinuação do tratamento devido a eventos adversos foram de 5,1% (6 mg), 7,7% (12 mg) e 10,3% (36 mg) para orforgliprona vs. 2,6% com placebo. As taxas gerais de descontinuação do tratamento foram de 21,9% (6 mg), 22,5% (12 mg) e 24,4% (36 mg) vs. 29,9% com placebo. Nenhum sinal de problemas na segurança hepática.
Os resultados detalhados do ATTAIN-1 serão apresentados no próximo mês na Reunião Anual da Associação Europeia para o Estudo da Diabetes (EASD) de 2025 e publicados em um periódico científico revisado por pares. Mais resultados do programa de estudos clínicos de fase 3 ATTAIN serão compartilhados ainda este ano, juntamente com achados do programa de estudos clínicos de fase 3 ACHIEVE, que avalia a orforgliprona em adultos com diabetes tipo 2.
Sobre a orforgliprona
A orforgliprona é uma molécula sintética (não peptídica) agonista do receptor do peptídeo semelhante ao glucagon-1 (GLP-1) oral, experimental, de dose única diária, que pode ser tomada a qualquer hora do dia sem restrições de alimentos e água3. A orforgliprona foi descoberta pela Chugai Pharmaceutical Co., Ltd. e licenciada pela Lilly em 2018. A Chugai e a Lilly publicaram os dados de farmacologia pré-clínica desta molécula juntas 4. A Lilly está conduzindo estudos de fase 3 sobre a orforgliprona para o tratamento do diabetes tipo 2 e para o controle de peso em adultos com obesidade ou sobrepeso com pelo menos uma comorbidade. A molécula também está sendo estudada como um tratamento potencial para apneia obstrutiva do sono e hipertensão em adultos com obesidade.
Sobre o ATTAIN-1 e o programa de estudos clínicos ATTAIN
ATTAIN-1 (NCT05869903) é um estudo de fase 3, de 72 semanas, randomizado, duplo-cego, controlado por placebo, que compara a eficácia e segurança de orforgliprona 6 mg, 12 mg e 36 mg como monoterapia com placebo em adultos com obesidade ou sobrepeso com pelo menos uma das seguintes comorbidades: hipertensão, dislipidemia, apneia obstrutiva do sono ou doença cardiovascular, sem diabetes. O estudo randomizou 3.127 participantes nos EUA, Brasil, China, Índia, Japão, Coreia, Porto Rico, Eslováquia, Espanha e Taiwan em uma proporção de 3:3:3:4 para receber 6 mg, 12 mg ou 36 mg de orforgliprona ou placebo. O desfecho primário do estudo foi demonstrar que a orforgliprona (6 mg, 12 mg, 36 mg) é superior na redução de peso corporal em relação ao período basal após 72 semanas, em comparação com placebo, em pessoas com IMC acima de ≥30,0 kg/m² ou IMC acima de ≥27,0 kg/m² com pelo menos uma comorbidade e histórico de pelo menos uma tentativa não sucedida auto reportada de perda de peso por meio de dieta. Todos os participantes nos braços de tratamento com orforgliprona iniciaram o estudo com uma dose de orforgliprona de 1 mg uma vez ao dia e, em seguida, aumentaram a dose de forma escalonada em intervalos de quatro semanas para sua dose de manutenção final randomizada de 6 mg (iniciado com 1 mg), 12 mg (fazendo o escalonamento de dose com 1 mg, 3 mg e 6 mg) ou 36 mg (fazendo o escalonamento de dose com 1 mg, 3 mg, 6 mg, 12 mg e 24 mg). A redução de dose só foi permitida para tolerabilidade gastrointestinal após outras mitigações falharem.
O programa de desenvolvimento clínico global de fase 3 ATTAIN para a orforgliprona recrutou mais de 4.500 pessoas com obesidade ou sobrepeso em dois estudos de registro globais. O programa começou em 2023, com resultados adicionais previstos para o final deste ano.
Sobre a Eli Lilly do Brasil
A Lilly é uma empresa de medicina que transforma a ciência em cura para melhorar a vida das pessoas em todo o mundo. Somos pioneiros em descobertas que mudam vidas há quase 150 anos e, hoje, nossos medicamentos ajudam mais de 51 milhões de pessoas em todo o mundo. Potencializando o poder da biotecnologia, química e medicina genética, seguimos avançando em novas descobertas para resolver alguns dos desafios de saúde mais importantes do mundo: redefinir o tratamento do diabetes; tratar a obesidade e reduzir seus efeitos devastadores de longo prazo; avançar na luta contra a doença de Alzheimer; oferecer soluções para alguns dos distúrbios mais debilitantes do sistema imunológico; e transformar os cânceres de tratamento mais difíceis em doenças controláveis. A cada passo em direção a um mundo mais saudável, somos motivados por uma coisa: melhorar a vida de milhões de pessoas. Isso inclui a realização de estudos clínicos inovadores que reflitam a diversidade do nosso mundo e trabalhar para garantir que nossos medicamentos sejam mais acessíveis aos pacientes. Para saber mais, acesse o site da Lilly do Brasil, e nossas redes sociais: Instagram, Facebook e LinkedIn.
Informações para imprensa
Ideal Axicom | lilly@ideal-axicom.com
Rafael Borges | rafael.borges@ideal-axicom.com | +55 (11) 97461-2757
Carolina Massaro | carolina.massaro@ideal-axixom.com | +55 (11) 99835-0594
Fábio Oliveira | fabio.oliveira@ideal-axicom.com | +55 (11) 98339-2678
Notas e Referências:
- A estimativa de eficácia representa a eficácia caso todos os participantes randomizados tivessem permanecido na intervenção do estudo (com possíveis interrupções de dose) durante as 72 semanas, sem iniciar tratamentos proibidos para controle de peso.
- A estimativa do regime de tratamento representa o efeito médio estimado do tratamento independentemente da adesão à intervenção do estudo ou do início de tratamentos proibidos para controle de peso.
- Ma X, Liu R, Pratt EJ, Benson CT, Bhattachar SN, Sloop KW. Effect of Food Consumption on the Pharmacokinetics, Safety, and Tolerability of Once-Daily Orally Administered Orforglipron (LY3502970), a Non-peptide GLP-1 Receptor Agonist. Diabetes Ther. 2024 Apr;15(4):819-832. doi: 10.1007/s13300-024-01554-1. Epub 2024 Feb 24. PMID: 38402332; PMCID: PMC10951152.
- T. Kawai, B. Sun, H. Yoshino, D. Feng, Y. Suzuki, M. Fukazawa, S. Nagao, D.B. Wainscott, A.D. Showalter, B.A. Droz, T.S. Kobilka, M.P. Coghlan, F.S. Willard, Y. Kawabe, B.K. Kobilka, & K.W. Sloop, Structural basis for GLP-1 receptor activation by LY3502970, an orally active nonpeptide agonist, Proc. Natl. Acad. Sci. U.S.A. 117 (47) 29959-29967, Link (2020).
Fonte: NK Consultoria.
Descubra mais sobre Biored Brasil
Assine para receber nossas notícias mais recentes por e-mail.
















